间歇性断食是一种通过周期性禁食与进食交替来激活细胞自噬、优化代谢健康并可能延缓衰老的饮食干预策略。其核心机制涉及禁食12-16小时后触发的代谢转换——从葡萄糖供能转向脂肪酸氧化和酮体生成,同时激活AMPK-mTOR自噬通路、提升生长激素和BDNF水平。
本报告基于最新临床研究证据,深入分析间歇性断食的生物学机制、健康益处、实践方法以及潜在风险,为医疗专业人员和健康管理从业者提供循证指导。
关键洞察
已证实的益处
新兴风险
肝糖原储备逐渐耗竭,机体启动从葡萄糖供能向脂肪酸氧化和酮体生成的代谢转换,此时自噬活性开始显著增强。 胰岛素水平下降与胰高血糖素水平上升构成激素环境变化的基础。AMPK因AMP/ATP比值升高而被激活,直接磷酸化ULK1,启动自噬体形成。 2021年《Nature》研究表明,仅在夜间开始禁食、持续至次日中午的个体才能获得寿命延长益处,而夜间进食者即使总禁食时间相同也无法获益。 禁食提升细胞内亚精胺水平,通过增强eIF5A活性促进自噬相关蛋白翻译,同时抑制mTOR和Akt等自噬抑制因子。 哥伦比亚大学研究证实,间歇性限时进食的延寿效果严格依赖于夜间特异性自噬诱导,这是iTRF介导寿命延长的核心机制。 通过PINK1-PARKIN通路选择性清除受损线粒体,减少活性氧产生,优化细胞能量代谢效率。
禁食状态下AMP/ATP比值升高激活AMPK,触发多重下游效应:抑制合成代谢,促进分解代谢,增强线粒体生物发生。 AMPK和SIRT1通过磷酸化和去乙酰化激活PGC-1α,促进线粒体DNA复制和呼吸链复合物组装。 禁食期间血浆胰岛素水平下降50-70%,胰岛素受体底物酪氨酸磷酸化增强,信号传导效率提升。 8-12周16:8限时进食可使HOMA-IR降低20-30%,效果与持续热量限制相当。
间歇性断食诱导GH脉冲式分泌增强,24小时总分泌量可增加2-3倍,夜间分泌峰值尤为显著。 • 促进脂肪组织脂解 • 刺激肝脏IGF-1合成 • 保护瘦体重 急性禁食期间,血浆皮质醇水平升高30-50%,促进糖异生、脂肪动员和蛋白质分解。 • 适应性应激反应 • 能量重分配 • 需避免慢性激活 禁食状态下BDNF表达上调2-3倍,促进海马神经发生、增强突触可塑性、改善学习记忆功能。 • 神经保护作用 • 认知功能改善 • 情绪调节效应核心生物学机制
1.1 细胞自噬激活
自噬启动条件与时间节点
12-16小时禁食期
分子调控机制
昼夜节律调控
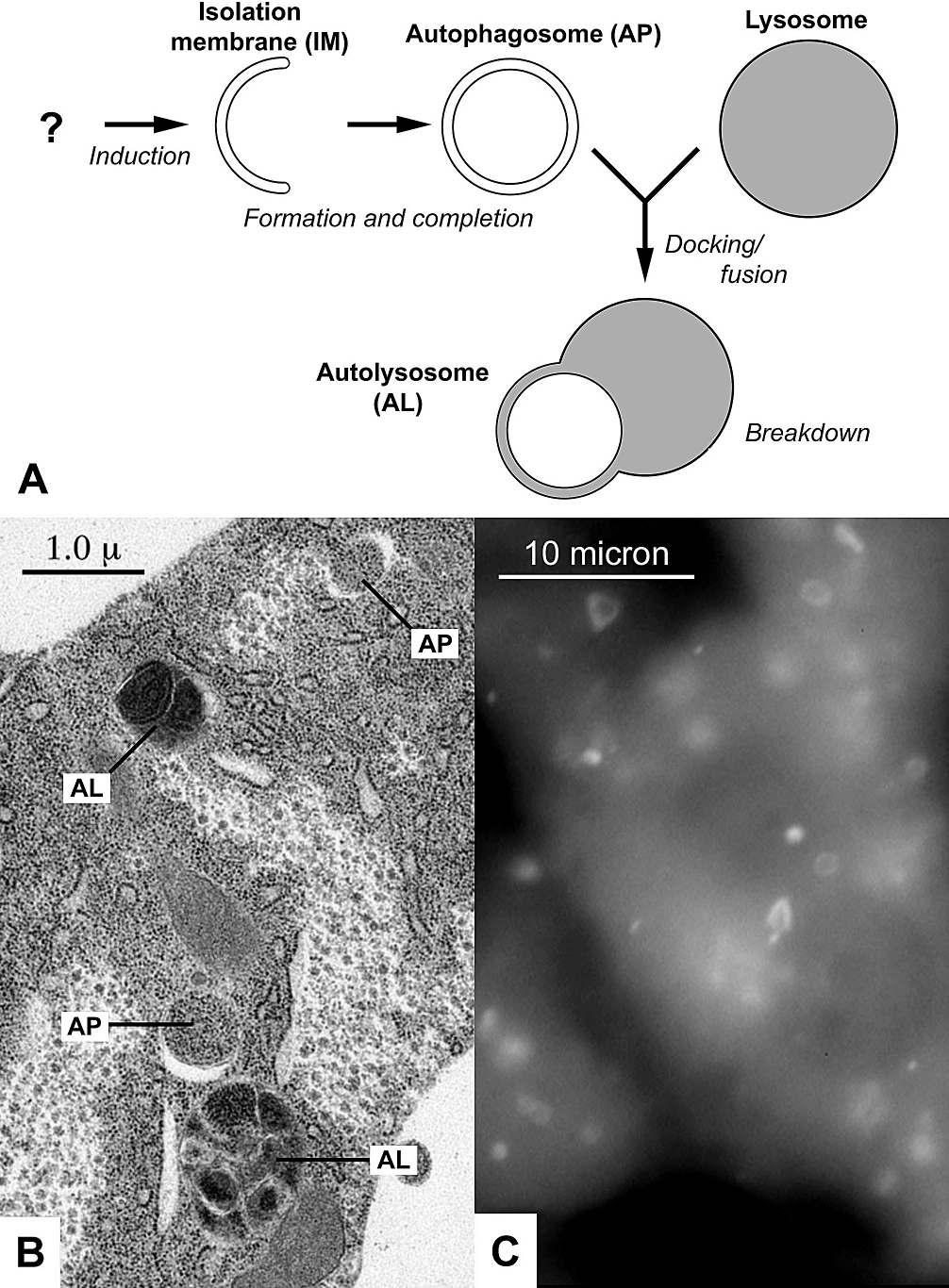
自噬的生理功能
自噬与抗衰老的分子关联
亚精胺介导途径
昼夜节律耦合
线粒体质量控制
1.2 代谢转换机制
能量底物转换过程
阶段
时间窗口
主要能量来源
关键代谢事件
饱腹状态
0-3小时
血液葡萄糖
胰岛素分泌,葡萄糖摄取和储存
餐后状态
3-12小时
肝糖原分解
胰高血糖素上升,糖异生增强
早期禁食
12-24小时
脂肪酸动员
激素敏感性脂肪酶激活,脂肪分解
深度禁食
24-48小时
酮体生成
肝脏β-氧化,BHB和AcAc大量产生
关键代谢通路
AMPK通路
PGC-1α介导
胰岛素敏感性改善
短期效应
临床证据
1.3 神经内分泌变化
生长激素分泌
HPA轴激活
BDNF上调
Aβ、α-突触核蛋白、过度磷酸化tau蛋白等神经退行性疾病特征性病理蛋白均为自噬底物。 PGC-1α介导的线粒体生物发生、PINK1-PARKIN介导的线粒体自噬、SIRT3介导的线粒体蛋白去乙酰化。 小胶质细胞向抗炎表型极化,促炎细胞因子释放减少,神经营养因子表达增加。 健康益处与临床证据
2.1 体成分优化与代谢健康
2.2 抗衰老与寿命延长
氧化应激调控
炎症抑制
细胞衰老延缓
跨物种寿命延长证据
物种
断食方案
寿命延长
关键机制
酵母
热量限制
2-3倍
TOR、Sch9通路抑制
线虫
间歇性禁食
50-100%
DAF-16/FOXO、HSF-1激活
果蝇
iTRF(夜间禁食)
18-25%
昼夜节律-自噬耦合
小鼠
隔日断食
10-30%
代谢转换、自噬激活
恒河猴
热量限制
未显著延长
疾病发病率降低
2.3 神经系统与认知功能
神经保护机制
自噬介导的蛋白清除
线粒体功能优化
神经炎症抑制
临床认知改善证据
禁食16小时(含夜间睡眠),进食窗口8小时 最常见安排:跳过早餐(12:00-20:00)或晚餐(08:00-16:00) 禁食14小时、进食10小时 适合初学者逐步适应,耐受性更好 6:00-15:00 或 9:00-17:00 更符合人体昼夜节律,代谢获益最优
停止夜间零食,早餐推迟1-2小时 预期:轻度饥饿,快速适应 进一步推迟早餐或提前晚餐 预期:饥饿感持续,能量波动 确定适合个人的进食窗口 预期:适应改善,精力提升 根据耐受性微调,建立长期习惯 预期:稳定执行,效果显现 目标每公斤目标体重1.2-1.6 g,优先选择鱼、禽、蛋、豆类、瘦肉 占总能量30-40%,以单不饱和和多不饱和脂肪为主 优先全谷物、豆类、非淀粉蔬菜,限制精制糖和加工食品实践方法与操作指南
3.1 主流断食模式详解
限时进食法(Time-Restricted Eating)
16/8法
14/10法
早段进食(eTRE)
周期性断食法
安全启动与适应策略
渐进式适应方案
第1-2周:12小时禁食
第3-4周:14小时禁食
第5-6周:16小时禁食
第7-8周:优化与巩固
进食期营养策略
蛋白质摄入
脂肪质量
碳水化合物
胎儿营养不足、低血糖、酮症风险;乳汁产量减少、婴儿发育影响 生长发育受阻、营养缺乏、骨发育和性成熟延迟 症状复发、饮食行为紊乱、限制性-暴食循环 酮症酸中毒、严重低血糖、死亡风险 降糖药物需调整,低血糖风险,需内分泌专科协作 运动表现下降、恢复受损、肌肉流失风险 药物-食物相互作用、吸收改变,需药师/医师评估长期影响与潜在风险
4.1 新兴风险证据
心血管风险争议
特殊人群禁忌与警示
绝对禁忌人群
妊娠期/哺乳期女性
18岁以下青少年儿童
进食障碍病史者
1型糖尿病患者
相对禁忌与医学监督需求
2型糖尿病患者
高强度运动员
长期服药者
绝大多数RCT持续8-16周,少数延长至6-12个月,5年以上数据极度匮乏 啮齿类动物代谢率、寿命、进食模式与人类差异显著,效应可能无法直接外推 盲法实施困难、失访率高、饮食自我报告偏倚,效应量可能被高估
体重稳步下降、代谢改善、精力提升 严重疲劳、月经紊乱、频繁感染、情绪恶化
间歇性断食作为一种饮食干预策略,具有明确的生物学机制和潜在健康益处,但2024-2026年涌现的新证据揭示了此前未被充分认识的免疫风险和心血管争议。
BHB介导的长寿浆细胞耗竭削弱疫苗保护效果,极端限时进食可能与心血管死亡风险增加相关——这些发现强调了"代谢物信号功能"和"肌肉保护"在断食效应中的核心地位。
理性态度是:既不盲目追捧,也不因噎废食;在充分知情、医学监督、个体化实施的前提下,探索适合自身的健康生活方式。
对于大多数人,温和的限时进食(12-14小时窗口,早段进食优先)、保证蛋白质充足、配合抗阻训练、关注整体饮食质量,可能是风险-获益比最优的实践路径。
综合评估与个性化建议
5.1 证据质量与研究方向
现有证据的局限性
时间维度
动物-人类转化
研究设计
优先研究议题
5.2 个体化决策框架
获益-风险评估矩阵
评估维度
获益倾向因素
风险倾向因素
决策建议
代谢健康
超重/肥胖、胰岛素抵抗、代谢综合征
体重正常或偏低、低血糖倾向、饮食失调史
代谢疾病高风险者更可能获益
免疫状态
慢性炎症性疾病、自身免疫病
频繁感染、免疫接种计划临近、免疫抑制治疗
疫苗需求高者谨慎,协调接种时机
生活方式
规律作息、社交需求可控、烹饪能力强
不规律工作时间、频繁社交聚餐、依赖外卖
选择灵活性高的方案(5:2)或调整时机
心理状态
良好自我调控、健康食物关系、明确健康目标
焦虑/抑郁、食物作为情绪调节、完美主义倾向
心理高风险者禁忌,优先心理支持
生命阶段
中年代谢下降期、更年期后
青春期、孕期/哺乳期、高龄(>75岁)
青少年和年轻成人避免长期严格断食
医学监督下的实施原则
基线评估
定期监测
动态调整
继续信号
终止信号
核心结论